Información de la convocatoria
Este Curso está acreditado por la Dirección Provincial de Educación y es puntuable para oposiciones y como mérito de formación permanente.
 MODALIDAD
MODALIDAD
Presencial.
OBJETIVOS
- Describir los métodos básicos de manipulación genética “in vitro” e “in vivo” de ADN recombinante, poniéndose especial énfasis en bases conceptuales y metodológicas de estas tecnologías, así como, de su alcance y aplicaciones más importantes.
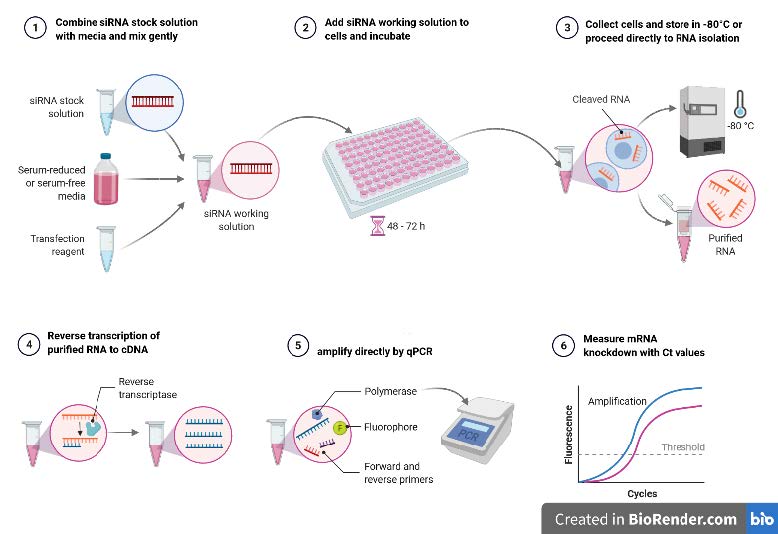
- Analizar las técnicas básicas de laboratorio para el aislamiento, purificación, amplificación mediante PCR y caracterización de fragmentos de ADN.
- Conocer como se estudian de los genomas.
PROGRAMA
- TEMA 1. INTRODUCCIÓN A LA INGENIERÍA GENÉTICA.
- Concepto de Ingeniería Genética. Hitos y evolución de la Ingeniería Genética.
- TEMA 2: PROCEDIMIENTOS PREPARATIVOS DE LOS ÁCIDOS NUCLEICOS.
- Función biológica de los ácidos nucleicos. Aislamiento de los ácidos nucleicos.
- Homogenización, separación y purificación. Métodos físicos, químicos y métodos enzimáticos de homogenización.
- Técnicas de separación y aislamiento más utilizadas. Extracción fenol-cloroformo.
- Precauciones Generales para el Aislamiento de Ácidos Nucleicos.
- TEMA 3: MÉTODOS ANALÍTICOS PARA DETERMINAR LA PUREZA Y CUANTIFICACIÓN DE LOS ÁCIDOS NUCLEICOS.
- Espectrofotometría.
- Sustancias cromóforos.
- Absorbancia y densidad óptica.
- Valor A260/A280.
- Valor A260/A230.
- Fluorescencia.
- Sustancias Fluoróforas.
- Agentes intercalantes: Catión etidio y alternativas.
- Electroforesis.
- Factores que influyen en la electroforesis.
- Electroforesis en geles de agarosa.
- Topología del ADN y recorrido electroforético.
- Electroforesis nativas y desnaturalizante en geles de acrilamida.
- TEMA 4: HERRAMIENTAS BÁSICAS EN LAS TECNOLOGÍAS DEL ADN RECOMBINANTE.
- Nucleasas (exonucleasas y endonucleasas), enzimas modificadoras de extremos, ligasas, polimerasas.
- Generación de ADN recombinante. Fragmentación del ADN.
- Enzimas de restricción: propiedades y aplicaciones. Ligación de extremos cohesivos y extremos romos.
- Ingeniería de extremos. Linkers, adaptadores.
- Métodos de ensamblaje de moléculas de ADN.
- Vectores de ADN.
- Tipos de Vectores. Vectores plasmídicos de clonado, de expresión y otros tipos de vectores.
- Clonación de vectores de expresión.
- Técnicas de clonación de secuencias de ADN.
- Técnicas de transformación, transfección y selección celular.
- TEMA 5: UTILIDADES DE LA HIBRIDACIÓN MOLECULAR Y LA PCR
- Síntesis y detección de sondas moleculares. Aplicaciones del método de Southern y la PCR para el diagnóstico molecular. Polimorfismos en la longitud de secuencias: minisatélites y microsatélites.
- Obtención de la huella molecular mediante el método de Southern y la PCR. Escrutinio de genotecas.
- Micromatrices de ADN. El perfil genético de los individuos mediante hibridación con micromatrices y secuenciación masiva.
- Perfiles genéticos y medicina personalizada. Detección de una secuencia en un cromosoma.
- Aplicaciones de las técnicas de hibridación in situ.
- TEMA 6: SECUENCIACIÓN, ANÁLISIS DE SECUENCIAS y MAPAS GENÉTICOS
- Principios generales de los procedimientos de determinación de la secuencia primaria de nucleótidos de una molécula de ADN.
- Histórico de los métodos de secuenciación.
- Secuenciación enzimática por el método de Sanger.
- Secuenciación semiautomatizada mediante detección fluorescente.
- Alternativas recientes al método de Sanger.
- Pirosecuenciación. Ultrasecuenciación.
- La era de la Genómica. Mapas genéticos y físicos.
- TEMA 7: ESTUDIO DE LA EXPRESIÓN GÉNICA
- Definición de patrones espacial y temporal de la expresión génica.
- Método de Northern. RTPCR semicuantitativa y cuantitativa (qRT-PCR).
- Análisis global de la expresión génica.
- Hibridación con micromatrices. Secuenciación masiva de ADNc (RNAseq).
- Localización de los productos de la expresión de un gen. Técnicas de hibridación in situ. Genes testigo.
- Construcciones para la determinación del patrón de expresión espacial de genes y la localización subcelular de proteínas.
- Métodos para la localización de secuencias reguladoras.
- Retraso en gel. Footprinting con DNasa I.
- TEMA 8: TRANSGÉNESIS Y MUTAGÉNESIS
- Genética “clásica” y Genética “inversa”.
- Mutagénesis clásica.
- Mutagénesis dirigida.
- Mutagénesis al azar mediante PCR.
- Inactivación dirigida de genes.
- Mutagénesis insercional y señalización de genes.
- Terapia génica.
- Construcciones antisentido.
- Mutagénesis mediante ARN interferente. microARN artificiales.
- Síntesis de polipéptidos a partir de fragmentos de ADN clonados.
- Vectores y genotecas de expresión.
- Estrategias para la expresión de un gen eucariótico en un hospedador procariótico: maduración de los transcritos y proteínas eucarióticas.
BREVE EXPLICACIÓN
Si quieres diseñar experimentos a nivel básico, comprendiendo las aplicaciones, la potencialidad, los límites reales y las estrategias metodológicas fundamentales en el campo de la manipulación génica, este curso te ayudará a realizarlo.
LUGAR
Facultad de Ciencias de la Salud.
PROFESORADO
Directores y ponentes del Curso:
- Dr. Darío Fernández Zoppino
- Dra. Natalia Busto Vázquez.
E-mail:
- dfx@ubu.es
- nbusto@ubu.es
CALENDARIO
Del 17 de enero al 4 de febrero de 2022.
- Martes, miércoles y jueves.
- De 9:30 a 14:30 horas.
DURACIÓN
54 horas.
NÚMERO DE ALUMNOS
Mínimo 10 y máximo 20 alumnos.
PRECIO
- Matrícula ordinaria: 150 €. Personas interesadas.
- Matrícula reducida: 135 €. Miembros de la comunidad universitaria de la UBU.
En el apartado de la matrícula se ofrece la opción de pago con TPV (pago mediante tarjeta de crédito).
Para realizar el pago mediante ingreso en la cuenta bancaria de la Universidad, deberá ponerse en contacto con Extensión Universitaria. Teléfono: 947 25 80 66
CRÉDITOS
2 créditos.



